На сегодняшний день не существует международно принятых обязательных правил проведения исследований на безопасность ГМ зерновых культур на животных с введением препарата с пищей. Хотя, руководства ОЭСР для проведения исследований безопасности химикатов являются разумной начальной точкой, существует острая необходимость создания международно принятых научно правильных экспериментальных разработок, особенно для оценки длительной безпасности ГМ культур.
Исследовании Сералии основывалось на экспериментальной разработке предыдущих исследований, проведенных индустрией в поддержку из заявления об регуляторной авторизации ГМО. Однако, он расширил проект исследования относительно времени проведения, ассортимента подопытных групп и широты проведения анатомических, клеточных и биохимических анализов. Поэтому, критика, обрушившаяся на исследование Сералини, в равной степени, если не больше, относится и к исследованию, проведенному индустрией, которое было намного уже.
Критики исследования Сералини, использовав двойные стандарты, признали промышленные исследования правильными, но полностью отвергли исследования Сералини. Критики должны использовать одинаковые стандарты, с помощью которых они признали исследование Сералини недействительным, к промышленным исследованиям. Единственным логическим выводом из такого сравнения является отрицание исследования Сералини и промышленного исследования или принятие того факта, что каждой исследование имеет свои заслуги относительно проведенных анализов.
Если будет сделан вывод, что оба исследования имеют свои заслуги, тогда необходимо обратиться к следующим фактам.
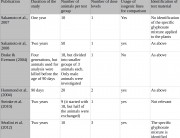
Те, кто продолжают спорить о том, что исследование Сералини является неприемлемым из-за использования слишком малого количества животных, должны обратиться к тому факту, что было использовано такое же количество животных, которое было проанализировано в ходе проверки химического состава крови и мои в 90-дневном исследовании Монсанто о безопасности ГМО, которое было признано.
Такое же количество животных считается достаточным ОЭСР для проведения некоторых исследований хронической токсичности индустрией для регуляторных целей. К примеру, в исследовании Сералини было использовано количество животных для проведения биохимического анализа крови и мочи в соответствии с ОЭСР протоколом 452, который может быть расширен до 2 лет.
Если открытия Сералини отклонены из-за недостаточного количества животных, тогда можно предположить, что токсические действия, обнаруженные в сравнении с промышленными исследованиями хронической токсичности, также проигнорированы и исследуемый продукт может быть выпущен на рынок. Если это правда, это будет большим сомнением общественности.
Критика, основанная на заявлении о том, что исследование Сералини является провальным карциногенным исследованием, является фиктивной. Исследование не было карциногенным, а исследованием хронической токсичности, в ходе которого были обнаружены опухоли.
Даже если и так, обобщенные заявления о том, что в длительных исследованиях необходимо использовать большое количество животных для обнаружения опухолей для того, чтобы считать такие исследования правомерными, являются подозрительными. Использование большого количества животных требуется, например, ОЭСР протоколом для проведения карциногенных исследований, необходимо для того, чтобы избежать получения «ложного негатива» — ложных выводов о безопасности. Это не относится к исследования Сералини, которое было направлено на выявление токсичности, а не безопасности. Если индустрия и инспекторы хотят поспорить о том, что открытия Сералини были «ложно положительными» — неправильный вывод о токсичности — они должны получить независимые токсикологические данные для того, чтобы это доказать.
Однако, мы судим сильные и слабые стороны исследования Сералини и определенные выводы являются ясными:
• Короткие 90-дневные исследования, проведенные индустрией, как часть их заявления для получения одобрения для продажи ГМ зерновых, являются недостаточными для определения токсического действия, которое может возникнуть в результате длительного (на протяжении всей жизни) потребления. Даже французские регулирующие агентства ANSES и HCB, которые критиковали исследование Сералини, пришли к выводу о необходимости проведения длительных исследований.
• ГМ индустрия и Европейское управление безопасности пищевых продуктов проигнорировала признаки токсичности, которые присутствовали в 90-дневном исследовании, как «биологически незначительные», что является неправильным.
• При оценке безопасности пестицидов недостаточно только проверить активный компонент (например, глифосат). Т.к. продается и используется продажная форма (раундап), она и должна быть исследована для получения обоснованных выводов.
• Длительные исследования (не менее 2 лет для грызунов) должны проводиться индустрией для всех ГМ пищевых продуктов и форм пестицидов — оба на рынке и в трубопроводах.
• Исследования ГМ зерновых должны быть направлены на выявление того, является ли отрицательное действие на здоровье результатом разрушительного действия процесса ГМ трансформации, процесса производства пестицидов или обоих.
• Для определения эффекта дозы необходимо использовать не менее 3 доз ГМ культуры и/или пестицида.
До тех пор, пока такие исследования не будут проведены, невозможно заявлять о том, что определенная ГМ культура является безопасной при длительном потреблении. В интересах безопасности Монсанто и другие разработчики ГМ семян и пестицидов не должны иметь доступа на рынок для недостаточно проверенной продукции. Законы должны быть переписаны и требовать проведения длительных и многонациональных исследований ГМ продукции и всех форм пестицидов перед началом их продаж; такие исследования должны финансироваться индустрией, но проводиться независимыми учеными.